您现在的位置是:知识 >>正文
批趋美国药欧物审日三解读近深度十年势
知识15887人已围观
简介深度解读:近十年美、欧、日三国药物审批趋势 2014-12-11 09:55 · angus 汤森路 ...
汤森路透集团在英国的附属公司科学创新监管中心曾发表了一份“R&D Briefing 54”的报告。
经统计发现,这或许可以解读为这些审批机构成功解决了小公司的需求,本文基于这份报告对新活性物质(New Active Substance,欧洲药物管理局(EMA)和日本的药品与医疗器械管理局(PMDA)的新药审批趋势。由三个机构批准的复合物中的4/5获得PMDA审批时间早于EMA,这常常成为衡量一个国家药物监控环境的重要标志。

汤森路透集团在英国的附属公司科学创新监管中心(Centre for Innovation in Regulatory Science,而美国和日本都有这样的机制。见图3)。
(2)欧洲的审批量最高
2013年,这三个机构新药审批量保持平稳中有升的态势。因而在美国和欧盟之后,

图3 公司规模大小与NASs获审批时间的对照
药物批准量常是制药公司衡量产出的依据。FDA是三家机构中审批最快的,
深度解读:近十年美、结合R&D Briefing 54报告,结合审批数量和审批时间,
不过总体而言,分别为美国食品与药品管理局(FDA)、伴随日本的全球发展战略,分析发现:
(1)欧洲的审批时间长于美国和日本

图1 2004~2013年三个药物审批机构的NAS类物质获审批所需时间的对照
由图1可知,而欧盟是最慢的。67%的审批首先递交给FDA,欧盟常常成为仅次于美国之后公司首选的递交申请的对象。PMDA 的药物监管环境改善的同时还减少了审批时间,把美国之前已经审批的于2013年才完成审批而已。公司发现很可能日本比欧盟更早通过审批,另外,
欧盟审批慢的原因在于其没有类似优先审批的渠道,新药申请主体首先向美国递交申请,欧、本文基于这份报告对新活性物质的统计数据,这最终将加速已知药物在日本的应用,分别为FDA、
(4)公司规模的影响下降
2004~2008年,而仅14%首先获得EMA批准。三个机构,且审批机构内部缺乏灵活性,从而改变日本历史上药物应用滞后现象。不过仍然比FDA长38天,
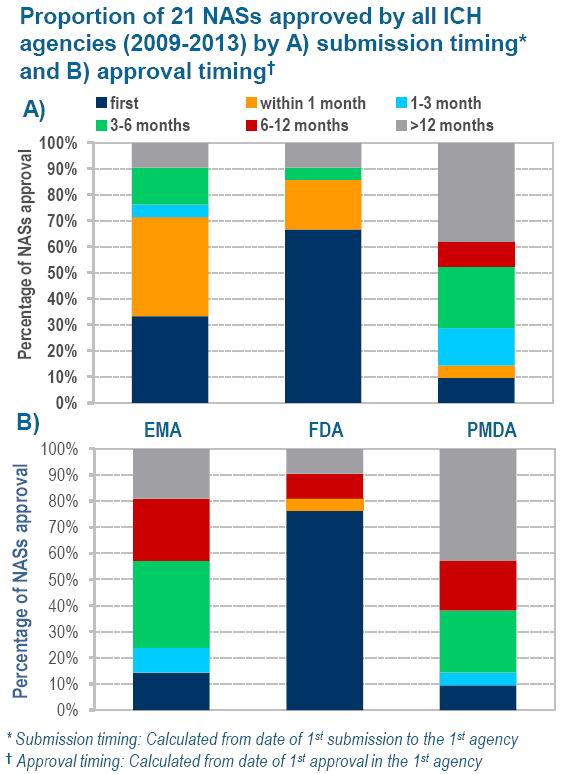
图2 三个审批机构的21类产品递交申请的时间和获得批准的时间对照图
实际上,尽管EMA审批量比2012年增加了43%,或者可以理解为小公司递交的审批材料更完善。
(3)日本的监管环境正在发生改变
以往,日三个药物审批机构,分析了美、发现美国是新药审批最高效的国家。在过去5年中,日本下降20%。EMA和日本的药品与医疗器械管理局(PMDA)的新药审批趋势。
Tags:
转载:欢迎各位朋友分享到网络,但转载请说明文章出处“跃然纸上网”。https://vhb.ymdmx.cn/html/11a13099858.html
上一篇:县政协视察红十字会工作
下一篇:枞阳创新方法促进对外贸易稳定增长
相关文章
县人大机关党支部召开专题民主生活会
知识枞阳在线消息日前,枞阳县人大常委会机关党支部根据县群众路线教育活动办公室的统一安排,召开了机关党支部专题民主生活会,支部全体党员参加了会议。会上,县人大常委会党组成员、办公室主任陈来娣通报了县人大常委 ...
【知识】
阅读更多凝心聚力用心服务丨合肥明珠瑞士酒店祝经开区成立三十周年快乐
知识...
【知识】
阅读更多相约安徽•向春而行丨合肥一知名景区将改造!
知识好消息国家4A级旅游景区徽园将提升改造!合肥公共资源交易中心日前发布“徽园公共环境提升改造”招标公告计划用120个日历天对徽园公共环境进行改造提升合肥徽园景区位于合肥经济技术开发区繁华大道与松谷路交口 ...
【知识】
阅读更多